Oddech życia: tlenoterapia w PARDS

Zespół ostrej niewydolności oddechowej u dzieci (ang. Pediatric Acute Respiratory Distress Syndrome, PARDS) to rodzaj ostrego uszkodzenia płuc, które występuje u ciężko chorych dzieci. Jest to ciężki stan zagrażający życiu, który rozwija się szybko i powoduje trudności w oddychaniu, obniżony poziom tlenu we krwi i niewydolność narządów. Jest podobny u analogicznego stanu u dorosłych, ale ma nieco inne definicje. Grupa Konferencyjna Pediatric Acute Lung Injury Consensus Conference Group (PALICC) postanowiła w 2015 r. opracować pediatryczne definicje zespołu ostrej niewydolności oddechowej wraz z zaleceniami dotyczącymi leczenia i przyszłych priorytetów badawczych. Wytyczne te zostały zaktualizowane w lutym 2023 r. z udziałem panelistów z 15 różnych krajów (1).
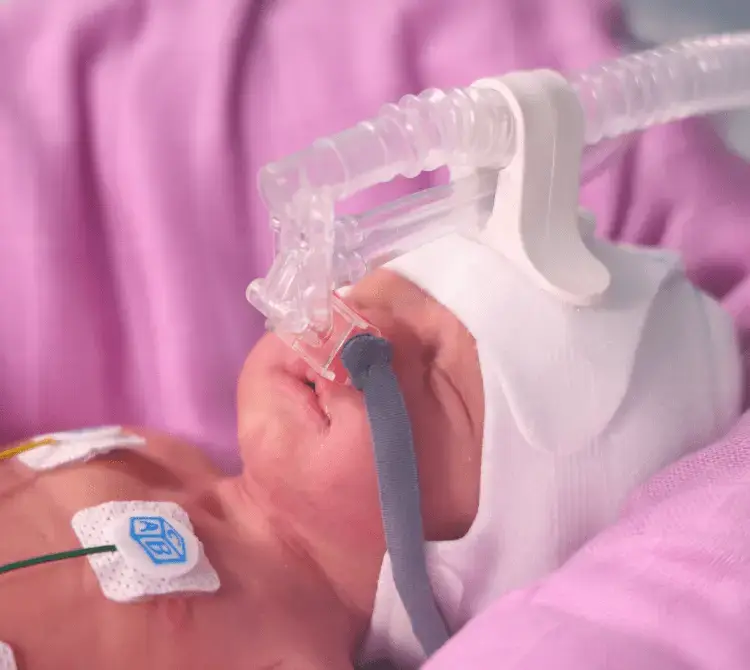
Ostatnio wiedza o (P)ARDS bardzo się wzbogaciła w wyniku powstania nowych koncepcji w patobiologii, ochronie płuc (ciśnienie napędowe, siła mechaniczna, P-SILI – uszkodzenie płuc pacjenta wywołane dużą różnicą ciśnień) oraz dzięki stosowaniu nowych technologii, takich jak tlenoterapia wysokoprzepływowa (ang. High Flow Oxygen Therapy, HFOT). W zaktualizowanych wytycznych PALICC-2 zmieniono definicję i kluczowe koncepcje leczenia związane z klasyfikowaniem stopnia PARDS co najmniej cztery godziny po wstępnym rozpoznaniu PARDS zarówno dla wentylacji inwazyjnej, jak i nieinwazyjnej (NIV), co pozwala na rozpoznanie „możliwego PARDS” u dzieci, u których stosuje się przeznosowe tryby wspomagania, takie jak HFOT (2).
Tradycyjnie zespół ostrej niewydolności oddechowej (ARDS) u dzieci rozpoznaje się na podstawie kryteriów American-European Consensus Conference (AECC). Globalnie przyjętą standardową definicją jest definicja berlińska z 2012 r. – została ona zmodyfikowana do stosowania w praktyce pediatrycznej.
Według wytycznych PALIC ARDS występuje w ciągu siedmiu dni od znanego urazu i jego stopień można ocenić za pomocą wskaźnika natlenienia (łagodny 4–8, umiarkowany 8–16 i ciężki >16) lub wskaźnika nasycenia tlenem (OSI). W przypadku rozpoznania PARDS, którego nie można inaczej wytłumaczyć siniczą chorobą serca, przewlekłą chorobą płuc i/lub dysfunkcją lewej komory.
Wytyczne PALICC-2 stanowią, że u wszystkich pacjentów w wieku poniżej 18 lat bez aktywnej okołoporodowej choroby płuc przy rozpoznaniu PARDS należy stosować kryteria PALICC-2; ponadto lekarze mogą stosować definicję PALICC-2 lub definicję noworodkową (Montreux NARDS) w przypadku noworodków oraz definicję PALICC-2 lub definicję dla osoby dorosłej (Berlin ARDS) w przypadku młodych dorosłych (1,2).
ARDS występuje u dzieci w różnym wieku i na różnym etapie rozwoju płuc i najczęściej jest spowodowany zapaleniem płuc, posocznicą i aspiracją. Może również wystąpić jako powikłanie w wyniku innych schorzeń i zabiegów, takich jak nowotwór, uraz, oparzenia, zapalenie trzustki, uraz inhalacyjny, transfuzja, krążenie pozaustrojowe, wrodzona choroba serca i choroby autoimmunologiczne. ARDS jest przyczyną znacznej chorobowości związanej z wtórnym zakażeniem, przedłużającą się hospitalizacją, neuropatią w stanie krytycznym i obniżeniem jakości życia w wyniku pogorszenia stanu zdrowia. Śmiertelność związana z ARDS u dzieci jest wysoka (10–12% w łagodnym lub umiarkowanym ARDS i 33% w ciężkich przypadkach (3). Badania dotyczące pediatrycznego ARDS wskazują na jego występowanie w około 1% do 4% wszystkich przyjęć na oddział intensywnej opieki pediatrycznej (PICU) (4-6).
Leczenie PARDS zazwyczaj rozpoczyna się od leczenia podstawowego procesu chorobowego; wytyczne PALLIC opisują również określone strategie wentylacji mechanicznej, takie jak docelowe objętości oddechowe 5–8 ml/kg należnej masy ciała (IBW) lub 3–6 ml/kg. W wytycznych omówiono również cele wymiany gazowej, sedację, blokadę nerwowo-mięśniową, inhalację tlenkiem azotu, stosowanie ułożenia na brzuchu, steroidy, wentylację oscylacyjną o wysokiej częstotliwości i ECMO (pozaustrojowe utlenowanie krwi). Omówiono również opiekę wspomagającą inną niż wspomaganie oddechu, która obejmuje takie formy leczenia jak gospodarka płynami, odżywianie, transfuzja krwi, sen i rehabilitacja.
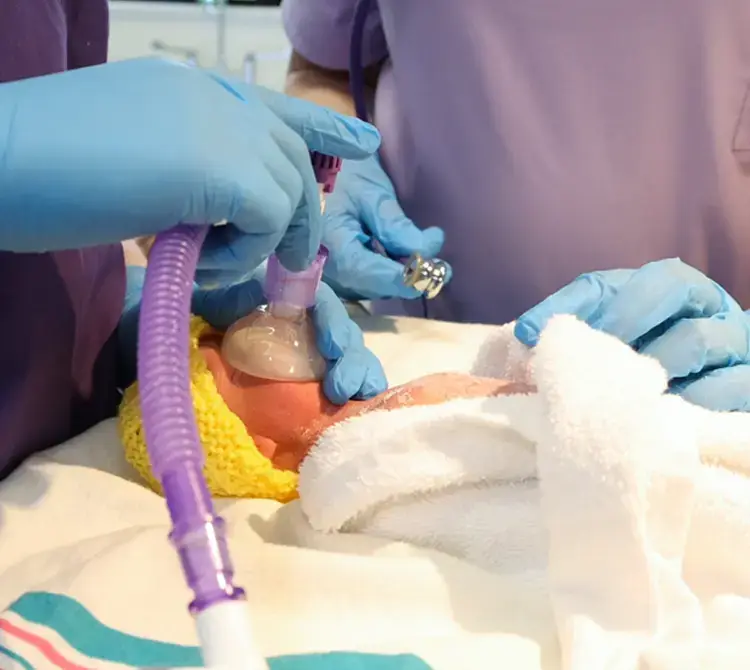
Należy zauważyć, że wentylacja nieinwazyjna (NIV) jest powszechnie stosowaną metodą leczenia niewydolności oddechowej u dzieci i może być korzystna w podgrupie pacjentów z PARDS o nasileniu od łagodnego do umiarkowanego. Konieczne jest jednak ścisłe monitorowanie pod kątem pogorszenia choroby i niepowodzenia wentylacji nieinwazyjnej (7). U pacjentów, u których stosuje się NIV, a którzy nie wykazują poprawy klinicznej w ciągu pierwszych sześciu godzin leczenia lub mają objawy podmiotowe i przedmiotowe pogorszenia choroby, w tym przyspieszoną częstość oddechów/tętna, zwiększony wysiłek oddechowy i pogorszenie wymiany gazowej (stosunek SpO2/FiO2), wytyczne zalecają intubację zamiast kontynuacji NIV. U pacjentów z możliwym PARDS lub zagrożonych PARDS podczas konwencjonalnej tlenoterapii lub HFOT, u których występują oznaki nasilenia niewydolności oddechowej, należy zastosować ograniczoną czasowo próbę NIV (CPAP lub BiPAP), jeśli nie ma jednoznacznych wskazań do intubacji.
Wczesne rozpoznanie i leczenie ma kluczowe znaczenie dla pacjentów zagrożonych PARDS, a wytyczne PALLICC-2 sugerują, że pacjentów poddawanych NIV z użyciem maski pełnotwarzowej (ciągłe dodatnie ciśnienie w drogach oddechowych [CPAP] lub dwupoziomowe dodatnie ciśnienie w drogach oddechowych [BiPAP]) z CPAP większym niż lub równym 5 cm H2O oraz osoby wentylowane inwazyjnie należy uznać za cierpiących na PARDS, jeśli spełniają kryteria czasu, utlenowania, etiologii/czynnika ryzyka i wyników obrazowania.
Próg natlenienia do rozpoznania możliwego PARDS u dzieci z przeznosowym wspomaganiem oddychania obejmuje dzieci, u których stosuje się ciągłe dodatnie ciśnienie w drogach oddechowych przez nos/dwupoziomowe dodatnie ciśnienie w drogach oddechowych, a które wymagają więcej niż 40% FiO2 do utrzymania nasycenia tlenem 88–97% oraz te, u których stosuje się tlenoterapię wysokoprzepływową przy minimalnych przepływach:
- <1 rok: 2 l/min
- 1–5 lat: 4 l/min
- 5–10 lat: 6 l/min
- >10 lat: 8 l/min
Zespół ostrej niewydolności oddechowej u dzieci (PARDS) to złożony i potencjalnie zagrażający życiu stan, który wymaga szybkiego rozpoznania i leczenia. Wczesne rozpoznanie i leczenie PARDS ma kluczowe znaczenie dla zapobiegania dalszemu pogorszeniu stanu zdrowia i zmniejszania śmiertelności. Chociaż poczyniono znaczne postępy w zrozumieniu i leczeniu PARDS, wiele kwestii, w tym patofizjologia schorzenia i najskuteczniejsze strategie leczenia, wymaga dalszych badań. Pomogą one lepiej zrozumieć PARDS i opracować skuteczniejsze opcje leczenia.
Ogólnie rzecz biorąc, PARDS jest złożonym i wymagającym schorzeniem, które wymaga wielodyscyplinarnego podejścia i specjalistycznej opieki. Jednak przy odpowiednim rozpoznaniu i właściwym leczeniu rokowanie dla wielu pacjentów z PARDS może być korzystne.
TABLE4. – Diagnosis of Pediatric Acute Respiratory Distress Syndrome (Definition Statement 1.1; Definition Statement 1.7.1) | ||||
|---|---|---|---|---|
Age (DS 1.1) | Exclude patients with perinatal lung disease | |||
Timing (DS 1.2) | Within 7 d of known clinical insult | |||
Origin of edema (DS 1.3) | Not fully explained by cardiac failure or fluid overload | |||
Chest imaging (DS 1.3) | New opacities (unilateral or bilateral) consistent with acute pulmonary parenchymal disease and which are not due primarily to atelectasis or pleural effusiona | |||
Oxygenation b (DS 1.4.1) | IMV: OI ≥ 4 or OSI ≥ 5 | |||
NIVc: Pao 2/Fio 2 ≤ 300 or Spo 2/Fio 2 ≤ 250 | ||||
Stratification of PARDS severity: Apply ≥ 4 hr after initial diagnosis of PARDS (DS 1.4.4) | ||||
IMV-PARDS: (DS 1.4.1) | Mild/moderate: OI < 16 or OSI < 12 (DS 1.4.5) | Severe: OI ≥ 16 or OSI ≥ 12 (DS 1.4.5) | ||
NIV-PARDSc (DS 1.4.2; DS 1.4.3) | Mild/moderate NIV-PARDS: Pao 2/Fio 2 > 100 or Spo 2/Fio 2 > 150 | Severe NIV-PARDS: Pao 2 /Fio 2 ≤ 100 or Spo 2 /Fio 2 ≤ 150 | ||
Special populations d | ||||
Cyanotic heart disease (DS 1.6.1; DS 1.6.2) | Above criteria, with acute deterioration in oxygenation not explained by cardiac disease | |||
Chronic lung disease (DS 1.6.3; DS 1.6.4) | Above criteria, with acute deterioration in oxygenation from baseline | |||
[1] Emeriaud G, López-Fernández YM, Iyer NP, Bembea MM, Agulnik A, Barbaro RP, Baudin F, Bhalla A, Brunow de Carvalho W, Carroll CL, Cheifetz IM, Chisti MJ, Cruces P, Curley MAQ, Dahmer MK, Dalton HJ, Erickson SJ, Essouri S, Fernández A, Flori HR, Grunwell JR, Jouvet P, Killien EY, Kneyber MCJ, Kudchadkar SR, Korang SK, Lee JH, Macrae DJ, Maddux A, Modesto I Alapont V, Morrow BM, Nadkarni VM, Napolitano N, Newth CJL, Pons-Odena M, Quasney MW, Rajapreyar P, Rambaud J, Randolph AG, Rimensberger P, Rowan CM, Sanchez-Pinto LN, Sapru A, Sauthier M, Shein SL, Smith LS, Steffen K, Takeuchi M, Thomas NJ, Tse SM, Valentine S, Ward S, Watson RS, Yehya N, Zimmerman JJ, Khemani RG; Second Pediatric Acute Lung Injury Consensus Conference (PALICC-2) Group on behalf of the Pediatric Acute Lung Injury and Sepsis Investigators (PALISI) Network. Executive Summary of the Second International Guidelines for the Diagnosis and Management of Pediatric Acute Respiratory Distress Syndrome (PALICC-2). Pediatr Crit Care Med. 2023 Feb 1;24(2):143-168. doi: 10.1097/PCC.0000000000003147. Epub 2023 Jan 20. PMID: 36661420; PMCID: PMC9848214. Executive Summary of the Second International Guidelines for… : Pediatric Critical Care Medicine (lww.com)
[2] Jouvet P, Thomas NJ, Willson DF, et al. Pediatric Acute Respiratory Distress Syndrome: Consensus Recommendations from the Pediatric Acute Lung Injury Consensus Conference. In: Pediatric Critical Care Medicine. ; 2015. doi:10.1097/PCC.0000000000000350. Pediatric Acute Respiratory Distress Syndrome: Consensus Rec… : Pediatric Critical Care Medicine (lww.com)
[3] Wong JJ-M, Jit M, Sultana R, et al. Mortality in Pediatric Acute Respiratory Distress Syndrome: A Systematic Review and Meta-Analysis. Journal of Intensive Care Medicine. 2019;34(7):563-571. doi:10.1177/0885066617705109 Mortality in Pediatric Acute Respiratory Distress Syndrome: A Systematic Review and Meta-Analysis – Judith Ju-Ming Wong, Mark Jit, Rehena Sultana, Yee Hui Mok, Joo Guan Yeo, Jia Wen Janine Cynthia Koh, Tsee Foong Loh, Jan Hau Lee, 2019 (sagepub.com)
[4] Erickson S, Schibler A, Numa A, et al. Acute lung injury in pediatric intensive care in Australia and New Zealand: a prospective, multicenter, observational study. Pediatr Crit Care Med. 2007;8(4):317–323 Acute lung injury in pediatric intensive care in Australia and New Zealand: a prospective, multicenter, observational study – PubMed (nih.gov)
[5] Dahlem P, van Aalderen WMC, Hamaker ME, Dijkgraaf MGW, Bos AP. Incidence and short-term outcome of acute lung injury in mechanically ventilated children. Eur Respir J. 2003;22(6):980–985. PubMed PMID: WOS:000187009900022. Incidence and short-term outcome of acute lung injury in mechanically ventilated children – PubMed (nih.gov)
[6] Wong JJ, Loh TF, Testoni D, Yeo JG, Mok YH, Lee JH. Epidemiology of pediatric acute respiratory distress syndrome in singapore: risk factors and predictive respiratory indices for mortality. Front Pediatr. 2014;2:78. PubMed PMID: 25121078. Pubmed Central PMCID: PMC4110624. Risk Stratification in Pediatric Acute Respiratory Distress Syndrome: A Multicenter Observational Study – PubMed (nih.gov)
[7] Orloff KE, Turner DA, Rehder KJ. The Current State of Pediatric Acute Respiratory Distress Syndrome. Pediatr Allergy Immunol Pulmonol. 2019;32(2):35-44. doi:10.1089/ped.2019.0999
[8] The Current State of Pediatric Acute Respiratory Distress Syndrome – PubMed (nih.gov)